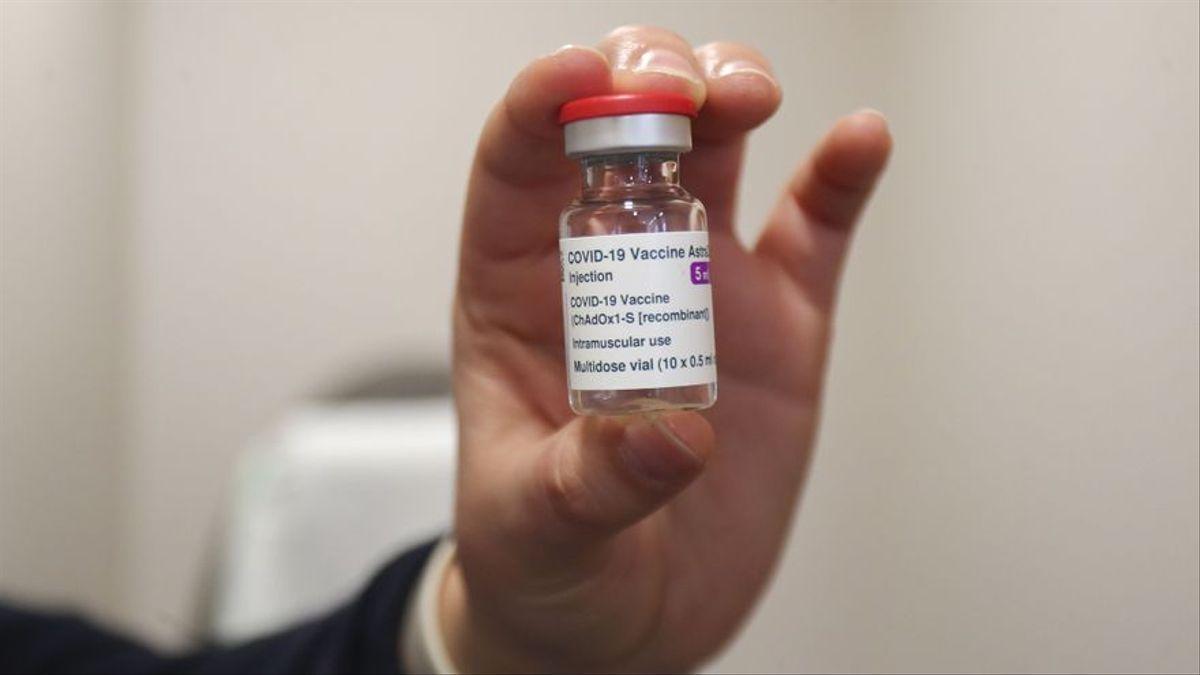
Tras una minuciosa revisión de los datos de seguridad disponibles, y en respuesta a la inquietud lanzada la semana pasada sobre los posibles efectos adversos de la inmunización británica contra el covid-19, AstraZeneca descarta que su vacuna aumente el riesgo de trombos o embolias. Así lo aclara la compañía en un comunicado de prensa emitido este mismo lunes para transmitir tranquilidad sobre la seguridad de su fórmula, que se reparte actualmente en toda la Unión Europea, España incluida.
El último estudio de seguridad realizado por la farmacéutica concluye que no existe ninguna evidencia de un aumento del riesgo de embolia pulmonar, trombosis venosa profunda (TVP) o trombocitopenia en ningún grupo de edad definido, sexo, lote o en ningún país concreto. Los datos indican que en estos primeros tres meses de campaña de vacunación solo se han detectado 15 casos de trombosis y 22 de embolia pulmonar entre los 17 millones de personas vacunadas entre la Unión Europea y el Reino Unido. Esta cifra es muy inferior a la que se esperaría que ocurriera de forma natural en una población general de este tamaño y es similar a la de otras vacunas autorizadas frente al covid-19, reafirma el comunicado.
La farmacéutica afirma que la prevalencia este tipo de efectos adversos también fue estudiada durante el proceso de estudios a gran escala. "En los ensayos clínicos, aunque el número de acontecimientos trombóticos fue pequeño, esta cifra fue más baja en el grupo vacunado. Tampoco ha habido ninguna evidencia de aumento de las hemorragias en los más de 60.000 participantes incluidos", añade la compañía en referencia a estos efectos adversos.
La naturaleza de la pandemia ha hecho que se preste una mayor atención a los casos individuales y estamos yendo más allá de las prácticas habituales de monitorización de la seguridad de los medicamentos autorizados al notificar los acontecimientos relacionados con la vacuna, para garantizar la seguridad pública, esgrime Ann Taylor, portavoz de AstraZeneca, en la nota de prensa remitida este lunes sobre la cuestión.
Lotes bajo inspección
AstraZeneca intenta responder así a la polémica levantada la semana pasada después de que varios países europeos decidieran pausar temporalmente la vacunación con un lote de la inmunización tras la detección de algunos casos de trombosis en vacunados. Mientras Dinamarca, Noruega e Islandia optaron por pausar durante catorce días la vacunación con esta fórmula; Italia, Estonia, Lituania, Letonia y Luxemburgo optaron por suspender el reparto de un lote concreto (el ABV5300). En España, Asturias, Andalucía y Castilla y León suspendieron la inmunización con el antígeno británico, mientras Cataluña retiró alrededor de 2.000 dosis sospechosas.
Sobre esta cuestión, la farmacéutica argumenta que, según su último análisis de seguridad, tampoco se han confirmado problemas relacionados con ningún lote de nuestra vacuna utilizado en Europa, ni en el resto del mundo. Nosotros mismos y las autoridades sanitarias europeas hemos realizado, y se siguen realizando, pruebas adicionales de manera independiente, y ninguna de estas pruebas ha demostrado ser motivo de preocupación, añaden. Asimismo, la empresa recuerda que las vacunas pasan por más de 60 controles de seguridad en manos de más de 20 laboratorios independientes. Todos los controles deben cumplir estrictos criterios de calidad y estos datos se envían a los organismos reguladores de cada país o región para que los revisen de forma independiente antes de que cualquier lote pueda ser distribuido a un país, afirman.
Todos estos datos, explica la compañía, están ahora en manos de la Agencia Europea del Medicamento (EMA) y se publicarán durante la próxima semana en su web. Asimismo, el organismo regulador debería pronunciarse sobre la cuestión en los próximos días, después de poner en marcha la semana pasada un estudio independiente sobre la cuestión. La primera impresión de la agencia es que, hoy por hoy, "la posición del comité de seguridad de la EMA es que los beneficios de las vacunas continúan superando los riesgos, por lo que la vacuna puede continuar administrándose".